
Como la reacción del electrodo para la especie química en solución ocurre en la interfaz de la solución (fase líquida) y el electrodo (fase sólida), en general se realiza a través de tres pasos elementales:
1) transferencia de masa de sustrato a la superficie del electrodo;
2) reacción de transferencia de electrones en la superficie del electrodo;
3) Difusión del producto desde el electrodo.
La velocidad de reacción del electrodo (corriente) se considera controlada por el proceso más lento. Es muy importante entender el proceso de control de funcionamiento del electrodo. Por ejemplo, si la actividad del propio catalizador de celda de combustible es lo suficientemente alta (la reacción de transferencia de electrones es rápida), el rendimiento de la celda puede mejorarse en gran medida diseñando un electrodo de transferencia de masa altamente eficiente (GDE).
El uso del sistema de electrodo de disco giratorio (RDE) puede controlar la velocidad de transferencia de masa para los procesos 1) y 3), de modo que la actividad del electrodo 2) se puede analizar cuantitativamente con suficiente reproducibilidad 1-2) .
Al combinar un electrodo de anillo con un electrodo de disco, la medición del electrodo de disco de anillo giratorio (RRDE) puede ayudar a detectar productos de reacción de RDE, sus productos intermedios, etc., de modo que se pueda analizar el mecanismo de reacción detallado 3) .
En esta nota técnica, aunque se omitió la fórmula teórica detallada y el método de análisis, se describió principalmente el experimento para RDE y RRDE, como los aparatos que utilizan para la medición de RDE y RRDE y los métodos experimentales básicos. Además, el método que adquiere los datos de la corriente de difusión limitante y el método de preparación de las parcelas de Levich y Kouteck-Levich se presentaron brevemente.
La característica de la voltimetría hidrodinámica (RDE, RRDE) es la medición electroquímica mientras el electrodo de trabajo está girando. Para obtener la tasa de transferencia de masa en buena reproducibilidad, es muy importante mantener el electrodo girando a una velocidad estable durante la medición. Por este medio, nos gustaría presentarle nuestro nuevo producto Rotador de electrodo RRDE-3A Aparato de electrodo de disco de anillo giratorio. Si el aparato de electrodo de disco de anillo giratorio RRDE-3A está equipado con un electrodo de disco giratorio (RDE) (que se muestra en la parte superior izquierda de la Figura 1), el electrodo de trabajo del disco puede girar durante la medición electroquímica.
Un electrodo de disco de anillo giratorio (RRDE) se muestra en la parte inferior izquierda de la Figura 1. El electrodo de disco está en la posición central, y una capa aislante delgada y un electrodo de anillo se ubican alrededor del electrodo de disco en forma de un círculo concéntrico. Cuando el electrodo RRDE está configurado para el aparato de electrodo de disco de anillo giratorio RRDE-3A, la medición del electrodo de disco de anillo giratorio se puede realizar fácilmente. Si tiene el aparato de electrodo de disco de anillo giratorio RRDE-3A, puede realizar mediciones RDE y RRDE fácilmente.
| Las especificaciones simples para el aparato de electrodo de disco de anillo giratorio RRDE-3A se describen a continuación: 1. Rango de rotación: 100 ∼ 8000 rpm 2. Precisión de rotación: <0.1% 3. Fuente de alimentación: 100 - 240 VCA; 50/60 Hz 4. Temperatura de funcionamiento: 10 - 50 ° C 5. Presión de gas de entrada: 5 psi máximo 6. Tamaño (W x D x H): 190 × 230 × 380 mm 7. Peso: 6 kg |
 Figura 1: RRDE-3A se usa para RDE (electrodo de disco giratorio) y RRDE (electrodo de disco de anillo giratorio) para las mediciones. |

Además de la función de rotación normal, la parte del motor puede estar al revés, de modo que el revestimiento de hilado se puede hacer fácilmente si se usa un tubo acrílico en conjunto. Esta función es bastante conveniente para la modificación del electrodo con catalizador.
Además, la función de purga de gas está equipada con el aparato de electrodo de disco de anillo giratorio RRDE-3A, el control manual del tiempo de purga está disponible, funciona con el analizador electroquímico ALS y también es posible el control remoto del tiempo de purga.


El contacto eléctrico entre el electrodo giratorio y el potenciostato se realiza a través de las escobillas de carbón de plata que entran en contacto con el eje de rotación. La figura 3 (a) muestra el eje conectado con el electrodo. El electrodo se puede quitar fácilmente girándolo con los dedos. Puede ver el eje sin electrodo en la Figura 3 (b), y las partes del disco y la punta del anillo están aisladas por PEEK. La punta del disco entra en contacto con el electrodo del disco, por lo que la corriente del disco pasa por el centro del eje y fluye hacia la parte superior del eje, como se muestra en la Figura 3 (c). La punta del anillo entra en contacto con el electrodo del anillo y la corriente del anillo fluye hacia la mitad del eje. Al usar dos pares del cepillo de carbón en contacto con las partes superior y media del eje (Figura 4), las corrientes de anillo y disco pueden fluir al potenciostato durante la rotación de los electrodos. Si las escobillas de carbón están gastadas, El ruido se producirá durante la medición. Si encuentra un ruido grave, compruebe primero el cepillo de carbón. Si el uso de las escobillas de carbón es demasiado grave, cámbielas.
1) AJ Bard y LR Faulkner. Fundamentos de métodos electroquímicos y aplicaciones, 2ª edición, Wiley, Nueva York (2001).
2) K. Oyaizu, M. Yuasa, et al. Electroquímica, 73, 1060 (2005).
3) K. Oyaizu, M. Yuasa, et al. Electroquímica., 74, 81 (2006).

La reacción redox con la velocidad de transferencia de electrones de la superficie del electrodo lo suficientemente más alta que la velocidad de difusión de la sustancia se denomina sistema reversible.
[Fe (CN) 6 3− / Fe (CN) 6 4− ] es un sistema reversible típico. En general, un sistema reversible para la medición de RDE puede ayudar a obtener el coeficiente de difusión D del sustrato, el potencial de medio pico reversible E 1/2 y el número de transferencia de electrones n.

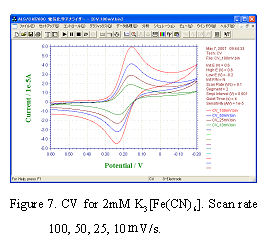
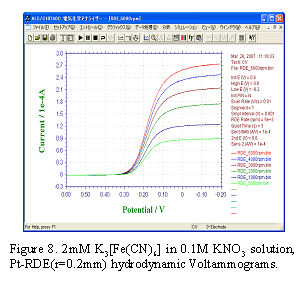

El proceso lento de transferencia de electrones en la superficie del electrodo se denomina sistema irreversible (no significa que no se produzca la reacción inversa). Un ejemplo de la reacción típica es la reducción de oxígeno disuelto en solución ácida.
La información obtenida de la medición de RDE para un sistema irreversible es la corriente controlada cinéticamente y el número de transferencia de electrones del catalizador Napp, que se puede calcular a partir de la pendiente de un gráfico de Koutecky-Levich en el caso del catalizador de electrodo.
Eq.5 se llama ecuación de Koutecky-Levich. El primer término en el lado derecho de la ecuación es la corriente de determinación de actividad que no depende de la velocidad de rotación. El segundo término es un recíproco de Eq.2 y significa la resistencia de transferencia de masa dependiendo de la velocidad de rotación.

4) M. Watanabe, Denki kagaku (actualmente electroquímica), 53, 671 (1985).
5) C.Paliteiro, A. Hamnett y JB Goodenough, J. Electroanal. Chem., 233, 147 (1987).

El electrodo RRDE, compuesto por electrodos de anillo y disco, se utiliza para RRDE-3A, como se muestra en la Fig.12. La rotación del electrodo se controla mediante RRDE-3A, y ambos potenciales (E D y E R ), desde el electrodo de anillo y el disco, se controlan de manera independiente mediante un electrodo de referencia común y un contraelectrodo. Las corrientes se registran mediante un potenciostato dual (analizador electroquímico de la serie 700C).
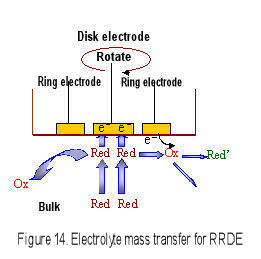

Cuando se rota el electrodo RRDE, la convección se produce cerca de la superficie del electrodo, por lo tanto, el espesor de la capa de difusión es constante y se observa la corriente limitada de difusión. Esta característica es la misma que RDE (la ecuación de Levich se usa para el sistema reversible). La ventaja para RRDE es que el producto electrolítico en el electrodo de disco se transporta al electrodo de anillo por la fuerza centrífuga y se detecta en el electrodo de anillo. El mecanismo de reacción electroquímica en el electrodo de disco se analiza con más detalle.

Para realizar una medición de RRDE cuantitativa, es necesario comprender la situación del transporte de especies electrolíticas desde el electrodo de disco al electrodo de anillo. El parámetro típico es la eficiencia de recolección N.
Si las siguientes reacciones ocurren en los electrodos de disco y anillo, las especies de Red se forman, el electrodo de disco se oxida en el electrodo de anillo, cuyo potencial se ha establecido en el potencial de oxidación de Red y se puede detectar como un corriente de anillo.
Sin embargo, una parte de la especie roja generada en el electrodo de disco puede escapar al volumen durante el transporte desde el electrodo de disco al electrodo de anillo (Fig. 15), y el | i D | > | i R| Se puede encontrar relación. La eficiencia de recolección se define como una relación del valor absoluto de la corriente de anillo a la corriente de disco (Ec. 6).
La eficiencia de recolección es una constante determinada solo por la configuración relativa y el tamaño de ambos electrodos y se puede calcular utilizando las ecuaciones teóricas que se muestran a continuación.
r 1 es el radio de un electrodo de disco, r 2 y r 3 son el radio interno y externo de un electrodo de anillo, respectivamente. Si r 1 = 0.2 cm, r 2 = 0.25 cm y r 3 = 0.35 cm se usan, la eficiencia de recolección calculada es 0.424.
Debido a que una superficie exacta del electrodo es desigual, la eficiencia de recolección real difícilmente sea una coincidencia con el valor de cálculo teórico. En general, los sistemas reversibles, como [Fe (CN) 6 ] 4− / [Fe (CN) 6 ] 3− , hidroquinona / benzoquinona, ferroceno 0 / + , Br- / Br 3 - y así sucesivamente se utilizan para la medición de la eficiencia de recolección de electrodos RRDE.
Veamos un ejemplo para medir la eficiencia de recolección. Se usó un electrodo de disco Pt ring-Pt ( r 1 = 0.2 cm, r 2 = 0.25 cm, r 3 = 0.35 cm) para la medición de RRDE. El electrodo RRDE se sumergió en 2 mmol / LK 3 [Fe (CN) 6 ] en 0,1 mol / L desolución de KNO 3 y se giró a una velocidad de rotación (por ejemplo, f = 300, 500, ……, 5000 rpm). El potencial de disco E Dse exploró de 0,6 V a -0,2 V frente a Ag / AgCl a una velocidad de exploración de 10 mV / s, potencial de anillo E Rse fijó a 0,6 V (el producto reducido [Fe (CN) 6 ] 4- se puede oxidar a este potencial), y los voltamogramas de potencial de corriente se registraron durante la rotación del electrodo. Fig.16 muestra la medida de RRDE. La relación de | i R-L | / | i D-L | es casi constante bajo varios ω. El promedio de eficiencia de recolección N es 0.422, este valor es bastante cercano al valor N calculado (0.424).

Anillo de Pt (ID = 5 mm, OD = 7 mm): el electrodo del disco GC (D = 4 mm) RRDE (pulido con alúmina y limpiado antes de su uso) se colocó en el rotador RRDE-3A y se colocó en la celda que estaba equipada con Ag / AgCl de referencia y contraelectrodos Pt. El electrolito era NaOH 1 M y la solución saturada de oxígeno se obtuvo mediante la purga O 2 gas durante 30 minutos (tiempo de purga fue controlada por el modo remoto RRDE-3A). El potencial se exploró en estado estático para comprender el rango de potencial adecuado para el electrodo de disco GC (el rango de potencial cambia con el material del electrodo).

Para la medición de RRDE, la tasa de exploración del potencial del disco se ajustó a 25 mV / s (según el experimento, también se utilizan 10, 5 mV / s), el potencial de anillo se ajustó a 0,1 V para que el producto de reducción de oxígeno H 2 O 2 El electrodo formado en el disco puede ser oxidado y detectado. Los voltamogramas se registraron mientras la exploración negativa potencial y la rotación del electrodo. Los voltamogramas de corriente de anillo y anillo obtenidos se muestran en la Fig. 18 (a) y (b), respectivamente.

En general, la reducción de oxígeno producida en el material de carbono en solución alcalina se expresa en las ecuaciones anteriores. Cuando el potencial se escanea a negativo, el oxígeno recibe 2 electrones ( k 2 ) y se cambia a HO 2 - . Si el potencial se escanea a más negativo, además se produce una reacción de 2 electrones (totalmente 4 electrones) ( k 3 ) y se forma OH - , la corriente aumenta y aparece la segunda onda. Además, la reacción química para HO 2 - desproporción en O 2 y OH - también se produce ( k 4 ). Potencial anillo se establece en 0,1 V de manera que la forma OH -Se oxida completamente y se detecta como corriente de anillo.
Con un potencial de disco de -0,5 V, la corriente de disco de la Fig. 18 (a) aumentó y la corriente de anillo correspondiente en la Fig. 18 (b) también aumentó. Sin embargo, cuando el potencial del disco fue escaneado a más negativo, por ejemplo, -1.0 V, la corriente del anillo disminuyó. Esto indicó que algunos de HO 2 - ion formado en el electrodo de disco era reducirse aún más para ser OH - y causó la corriente de anillo decreciente. De esta forma se analizan por detección en electrodo de anillo, producto de reacción de disco y mecanismo de reacción. Los datos en la Fig. 18 no son tan ideales; en la referencia 5) cuando se usó un electrodo de disco de grafito pirolítico (plano del borde) en anillo Pt, la reducción de los electrones de la segunda onda 4 se realizó completamente, y k 1, k 2 y k 3 fueron analizados cuantitativamente.
En los últimos años, la reducción catalítica catódica de oxígeno relacionada con la investigación de celdas de combustible ha atraído mucha atención. El platino o una aleación de platino se usa a menudo como catalizador de electrodo para el electrodo de combustible o el electrodo de oxígeno. Los trabajos de investigación con respecto al catalizador de reemplazo de platino están activos para reducir el costo de desarrollo de las celdas de combustible 6) . Por ejemplo, se produjo una reducción de oxígeno de 4 o 2 electrones en el electrodo de disco en una solución alcalina. La reducción de 2 electrones intermedio HO 2 - fue transportado al electrodo de anillo por rotación y no se detectó en el electrodo de anillo por oxidación (Fig.19).
Fig. 19 La imagen de la reacción catalítica se produce en el electrodo de disco de anillo giratorio.

Las mediciones de voltametría hidrodinámica RDE y RRDE pueden obtener la corriente constante mediante la rotación del electrodo, lo que causa convección cerca de la superficie del disco y controla el espesor de la capa de difusión. El mecanismo de reacción electroquímica para sistemas reversibles e irreversibles se puede analizar cambiando la velocidad de rotación. Especialmente, el RRDE se puede utilizar para estudios de aplicaciones de amplio rango 7-10) , como la reacción del catalizador de celda de combustible, el metal, la disolución de aleaciones y el análisis del mecanismo de galvanoplastia, la síntesis electroorgánica, la reacción óptica, etc. Como la voltametría hidrodinámica, RDE y RRDE pueden ayudar a Adquirir mucha información electroquímica, se esperan muchas más aplicaciones en el futuro.
5) C.Paliteiro, A. Hamnett y JB Goodenough, J. Electroanal. Chem., 233, 147 (1987).
6) H. Meng, PK Shen, Electroquímica Communication, 8, 588, (2006).
7) T. Ousaka, S. Oyama, T. Ohsaka, Métodos electroquímicos, Koudansha, Japón (1989).
8) A. Fujishima y K. Honda, Denki Kagaku (electroquímica), 42, 213 (1974).
9) M. Watanabe y H. Uchida, Electroquímica, 68, 816 (2000).
10) K. Tokuda y T. Ohsaka, Denki Kagaku (electroquímica), 61, 193 (1993).